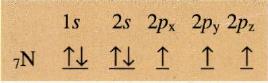Αρχές δόμησης πολυηλεκτρονικών ατόμων
Στο άτομο του υδρογόνου, το μοναδικό ηλεκτρόνιο τοποθετείται στο τροχιακό 1s. Στην περίπτωση αυτή λέμε πως το άτομο βρίσκεται στη θεμελιώδη του κατάσταση. H τοποθέτηση του σε οποιαδήποτε άλλο τροχιακό είναι δυνατή μετά από διέγερση του ατόμου.
Στα πολυηλεκτρονικά άτομα προφανώς τα πράγματα είναι πιο πολύπλοκα.
H συμπλήρωση των τροχιακών με ηλεκτρόνια, η λεγόμενη ηλεκτρονιακή δόμηση, ακολουθεί ορισμένους κανόνες (αρχές) τους οποίους αναπτύσσουμε παρακάτω.
Τέλος, να υπογραμμίσουμε ότι ηλεκτρονιακή δόμηση έχει θεμελιώδη σημασία, γιατί με βάση αυτή διαμορφώνεται η ηλεκτρονιακή δομή των ατόμων και κατ' επέκταση η χημική συμπεριφορά τους.
Απαγορευτική αρχή του Pauli
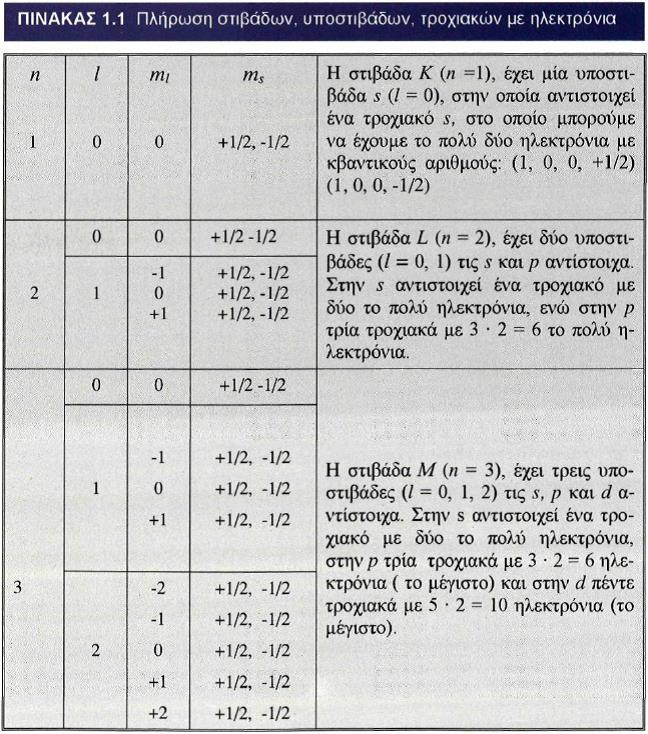
> Σύμφωνα με την απαγορευτική αρχή του Pauli είναι αδύνατο να υπάρχουν στο ίδιο άτομο δύο ηλεκτρόνια με ίδια τετράδα κβαντικών αριθμών (n, l, ml, ms). Συνεπώς, δεν μπορεί ένα τροχιακό να χωρέσει πάνω από δύο ηλεκτρόνια
Με βάση αυτή την αρχή προκύπτει ο μέγιστος αριθμός ηλεκτρονίων που έχει μια υποστιβάδα και μια στιβάδα, όπως φαίνεται στον πίνακα:
Στο άτομο του υδρογόνου, το μοναδικό ηλεκτρόνιο τοποθετείται στο τροχιακό 1s. Στην περίπτωση αυτή λέμε πως το άτομο βρίσκεται στη θεμελιώδη του κατάσταση. H τοποθέτηση του σε οποιαδήποτε άλλο τροχιακό είναι δυνατή μετά από διέγερση του ατόμου.
Στα πολυηλεκτρονικά άτομα προφανώς τα πράγματα είναι πιο πολύπλοκα.
H συμπλήρωση των τροχιακών με ηλεκτρόνια, η λεγόμενη ηλεκτρονιακή δόμηση, ακολουθεί ορισμένους κανόνες (αρχές) τους οποίους αναπτύσσουμε παρακάτω.
Τέλος, να υπογραμμίσουμε ότι ηλεκτρονιακή δόμηση έχει θεμελιώδη σημασία, γιατί με βάση αυτή διαμορφώνεται η ηλεκτρονιακή δομή των ατόμων και κατ' επέκταση η χημική συμπεριφορά τους.
Απαγορευτική αρχή του Pauli
> Σύμφωνα με την απαγορευτική αρχή του Pauli είναι αδύνατο να υπάρχουν στο ίδιο άτομο δύο ηλεκτρόνια με ίδια τετράδα κβαντικών αριθμών (n, l, ml, ms). Συνεπώς, δεν μπορεί ένα τροχιακό να χωρέσει πάνω από δύο ηλεκτρόνια
Με βάση αυτή την αρχή προκύπτει ο μέγιστος αριθμός ηλεκτρονίων που έχει μια υποστιβάδα και μια στιβάδα, όπως φαίνεται στον πίνακα:

Με τον ίδια λογική προκύπτει ότι η στιβάδα N (n = 4), έχει 4 υποστιβάδες (l = 0, 1,2, 3) τις s, p, d,f, αντίστοιχα και η τέταρτη υποστιβάδα (f) έχει 7 τροχιακά (ml = -3, -2, -1, 0, +1, +2, +3) με μέγιστο αριθμό ηλεκτρονίων 2 · 7 = 14.
Στο πίνακα 1.2 φαίνεται ο μέγιστος αριθμός ηλεκτρονίων που έχει μια στιβάδα και μια υποστιβάδα.
Να παρατηρήσουμε ότι δεν υπάρχουν ηλεκτρόνια σε υποστιβάδες 5g ή 6f κλπ σε μη διεγερμένα άτομα.
Στο πίνακα 1.2 φαίνεται ο μέγιστος αριθμός ηλεκτρονίων που έχει μια στιβάδα και μια υποστιβάδα.
Να παρατηρήσουμε ότι δεν υπάρχουν ηλεκτρόνια σε υποστιβάδες 5g ή 6f κλπ σε μη διεγερμένα άτομα.
Αρχή ελάχιστης ενέργειας
Κατ' αρχάς θα πρέπει να θυμίσουμε ότι οι εξισώσεις Schrodinger μπορούν να επιλυθούν ακριβώς μόνο στην περίπτωση του υδρογόνου και των υδρογονοειδών (ιόντων με ένα μόνο ηλεκτρόνιο π.χ. He+, Li2+ κλπ ).
Οι κβαντικοί αριθμοί εφαρμόζονται κατά προσέγγιση (και όχι «άνετα») στα πολυ-ηλεκτρονικά άτομα καθώς η εξίσωση Schrodinger δεν λύνεται ακριβώς για τα πολυηλεκτρονικά άτομα. Λύνεται με διάφορες προσεγγιστικές μεθόδους οπότε οι κβαντικοί αριθμοί συμβολίζονται με τον υδρογονοειδή τρόπο έχοντας όμως κατά νου τις προσεγγίσεις που έχουν γίνει.
Παρόλα αυτά έχει αποδειχτεί ότι η μορφή των τροχιακών στα πολυηλεκτρονικά άτομα δε διαφέρει αισθητά απ' αυτήν που περιγράφηκε για το άτομο του υδρογόνου.
Αντίθετα, υπάρχει διαφορά στη διαδοχή των ενεργειακών σταθμών του ηλεκτρονίου.
Για να γίνουμε σαφείς, σ' ένα πολυηλεκτρονικό άτομο, πλην των ελκτικών δυνάμεων πυρήνα - ηλεκτρονίου (που καθορίζονται από τον κύριο κβαντικό αριθμό), ασκούνται απώσεις ηλεκτρονίου - ηλεκτρονίου (που καθορίζονται από το δευτερεύοντα κβαντικό αριθμό).
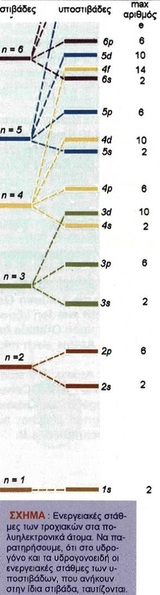
Για το λόγο αυτό διαφοροποιούνται οι ενεργειακές στάθμες των υποστιβάδων της ίδιας στιβάδας, όπως φαίνεται στο διπλανό σχήμα.
> Σύμφωνα με την αρχή της ελάχιστης ενέργειας, κατά την ηλεκτρονιακή δόμηση ενός πολυηλεκτρονικού ατόμου, τα ηλεκτρόνια οφείλουν να καταλάβουν τροχιακά με τη μικρότερη ενέργεια, ώστε να αποκτήσουν τη μεγίστη σταθερότητα στη θεμελιώδη κατάσταση.
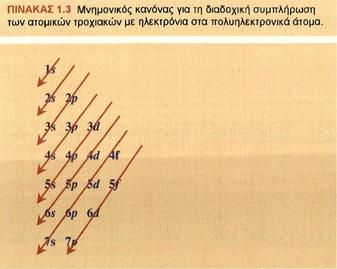
Επειδή δύσκολα μπορεί να θυμηθεί κανείς το διάγραμμα διαδοχής των ενεργειακών σταθμών, που παρατίθεται παραπλεύρως, δίνεται ένα μνημονικό διάγραμμα.
Στο διάγραμμα αυτό, η συμπλήρωση των τροχιακών ακολουθεί μια - μια, με τη σειρά τις διαγώνιες, με τη φορά που δείχνουν τα βέλη.
Κατ' αυτό τον τρόπο δομείται ηλεκτρονιακά το άτομο στη θεμελιώδη του κατάσταση.
Κατ' αρχάς θα πρέπει να θυμίσουμε ότι οι εξισώσεις Schrodinger μπορούν να επιλυθούν ακριβώς μόνο στην περίπτωση του υδρογόνου και των υδρογονοειδών (ιόντων με ένα μόνο ηλεκτρόνιο π.χ. He+, Li2+ κλπ ).
Οι κβαντικοί αριθμοί εφαρμόζονται κατά προσέγγιση (και όχι «άνετα») στα πολυ-ηλεκτρονικά άτομα καθώς η εξίσωση Schrodinger δεν λύνεται ακριβώς για τα πολυηλεκτρονικά άτομα. Λύνεται με διάφορες προσεγγιστικές μεθόδους οπότε οι κβαντικοί αριθμοί συμβολίζονται με τον υδρογονοειδή τρόπο έχοντας όμως κατά νου τις προσεγγίσεις που έχουν γίνει.
Παρόλα αυτά έχει αποδειχτεί ότι η μορφή των τροχιακών στα πολυηλεκτρονικά άτομα δε διαφέρει αισθητά απ' αυτήν που περιγράφηκε για το άτομο του υδρογόνου.
Αντίθετα, υπάρχει διαφορά στη διαδοχή των ενεργειακών σταθμών του ηλεκτρονίου.
Για να γίνουμε σαφείς, σ' ένα πολυηλεκτρονικό άτομο, πλην των ελκτικών δυνάμεων πυρήνα - ηλεκτρονίου (που καθορίζονται από τον κύριο κβαντικό αριθμό), ασκούνται απώσεις ηλεκτρονίου - ηλεκτρονίου (που καθορίζονται από το δευτερεύοντα κβαντικό αριθμό).
Για το λόγο αυτό διαφοροποιούνται οι ενεργειακές στάθμες των υποστιβάδων της ίδιας στιβάδας, όπως φαίνεται στο διπλανό σχήμα.
> Σύμφωνα με την αρχή της ελάχιστης ενέργειας, κατά την ηλεκτρονιακή δόμηση ενός πολυηλεκτρονικού ατόμου, τα ηλεκτρόνια οφείλουν να καταλάβουν τροχιακά με τη μικρότερη ενέργεια, ώστε να αποκτήσουν τη μεγίστη σταθερότητα στη θεμελιώδη κατάσταση.
Επειδή δύσκολα μπορεί να θυμηθεί κανείς το διάγραμμα διαδοχής των ενεργειακών σταθμών, που παρατίθεται παραπλεύρως, δίνεται ένα μνημονικό διάγραμμα.
Στο διάγραμμα αυτό, η συμπλήρωση των τροχιακών ακολουθεί μια - μια, με τη σειρά τις διαγώνιες, με τη φορά που δείχνουν τα βέλη.
Κατ' αυτό τον τρόπο δομείται ηλεκτρονιακά το άτομο στη θεμελιώδη του κατάσταση.

Ας δούμε για παράδειγμα, πως κατανέμονται τα 26 ηλεκτρόνια στο άτομο του σιδήρου, στη θεμελιώδη του κατάσταση.
Πρώτα τοποθετούνται δύο ηλεκτρόνια στην υποστιβάδα 1s, και γράφουμε 1s2,
μετά τοποθετούμε δύο ηλεκτρόνια στην υποστιβάδα 2s (1s2 2s2),
ακολουθούν έξι ηλεκτρόνια στην υποστιβάδα 2p (1s2 2s2 2p6),
δύο ηλεκτρόνια στην υποστιβάδα 3s (1s2 2s2 2p6 3s2),
έξι στην υποστιβάδα 3p (1s2 2s2 2p6 3s2 3p6)
και δύο στην 4s (1s2 2s2 2p6 3s2 3p6 4s2).
Τα τελευταία έξι ηλεκτρόνια πάνε στην υποστιβάδα 3d, η οποία χωράει συνολικά δέκα ηλεκτρόνια.
Έτσι, η ηλεκτρονιακή δομή του σιδήρου είναι:
Πρώτα τοποθετούνται δύο ηλεκτρόνια στην υποστιβάδα 1s, και γράφουμε 1s2,
μετά τοποθετούμε δύο ηλεκτρόνια στην υποστιβάδα 2s (1s2 2s2),
ακολουθούν έξι ηλεκτρόνια στην υποστιβάδα 2p (1s2 2s2 2p6),
δύο ηλεκτρόνια στην υποστιβάδα 3s (1s2 2s2 2p6 3s2),
έξι στην υποστιβάδα 3p (1s2 2s2 2p6 3s2 3p6)
και δύο στην 4s (1s2 2s2 2p6 3s2 3p6 4s2).
Τα τελευταία έξι ηλεκτρόνια πάνε στην υποστιβάδα 3d, η οποία χωράει συνολικά δέκα ηλεκτρόνια.
Έτσι, η ηλεκτρονιακή δομή του σιδήρου είναι:
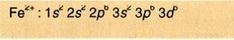
Να παρατηρήσουμε στην παραπάνω ηλεκτρονιακή δομή ότι γράφουμε πρώτα την 3d και μετά την 4s, παρόλο που η υποστιβάδα 4s συμπληρώθηκε πρώτη, σύμφωνα με την αρχή ελάχιστης ενέργειας.
Αυτό συμβαίνει επειδή μετά την εισαγωγή ηλεκτρονίων στην υποστιβάδα 3d αυτή αποκτά λιγότερη ενέργεια από την 4s.
Ανάλογα ισχύει και για τις 4d και 5s .
Για τον ίδιο λόγο κατά τον ιοντισμό του Fe σε Fe2+ αποβάλλονται τα 4s και όχι τα 3d ηλεκτρόνια. Δηλαδή, η ηλεκτρονιακή δομή του ιόντος Fe + είναι:
Αυτό συμβαίνει επειδή μετά την εισαγωγή ηλεκτρονίων στην υποστιβάδα 3d αυτή αποκτά λιγότερη ενέργεια από την 4s.
Ανάλογα ισχύει και για τις 4d και 5s .
Για τον ίδιο λόγο κατά τον ιοντισμό του Fe σε Fe2+ αποβάλλονται τα 4s και όχι τα 3d ηλεκτρόνια. Δηλαδή, η ηλεκτρονιακή δομή του ιόντος Fe + είναι:

Av γράψουμε τα ηλεκτρόνια σε στιβάδες και όχι σε υποστιβάδες έχουμε:
Τέλος, να σημειώσουμε ότι σε ορισμένες περιπτώσεις η κατανομή των ηλεκτρονίων δεν είναι αυτή που προβλέπεται, με βάση τις αρχές δόμησης.
Π.χ. η ηλεκτρονιακή δομή του 24Cr είναι (2-8-13-1) και όχι (2-8-12-2).
Οι περιπτώσεις όμως αυτές ξεφεύγουν από τα όρια μελέτης μας.
Τέλος, να σημειώσουμε ότι σε ορισμένες περιπτώσεις η κατανομή των ηλεκτρονίων δεν είναι αυτή που προβλέπεται, με βάση τις αρχές δόμησης.
Π.χ. η ηλεκτρονιακή δομή του 24Cr είναι (2-8-13-1) και όχι (2-8-12-2).
Οι περιπτώσεις όμως αυτές ξεφεύγουν από τα όρια μελέτης μας.
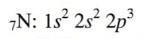
Κανόνας του Hund
Παρόλο που έχουμε ήδη δώσει παραδείγματα ηλεκτρονιακής δόμησης, εντούτοις παραμένουν αδιευκρίνιστα ορισμένα σημεία
Στο παράδειγμα του Fe, δεν ξέρουμε πως ακριβώς κατανέμονται τα 6 ηλεκτρόνια στα 3d τροχιακά.
Γνωρίζουμε ότι η συνολική χωρητικότητα των 3d είναι 10 ηλεκτρόνια, αλλά δεν γνωρίζουμε αν μένει ή όχι κάποιο d τροχιακό κενό.
Την απάντηση σ' αυτού του είδους τα ερωτήματα δίνει ο κανόνας του Hund από τον οποίο προκύπτει:
> «Ηλεκτρόνια που καταλαμβάνουν τροχιακά της ίδιας ενέργειας (της ίδιας υποστιβάδας) έχουν κατά προτίμηση παράλληλα spin».
Για παράδειγμα στο άτομο του αζώτου 7Ν η κατανομή σε υποστιβάδες είναι:
ή αναλυτικότερα, αν θέλουμε να δείξουμε την κατανομή των ηλεκτρονίων στα τροχιακά:
Παρόλο που έχουμε ήδη δώσει παραδείγματα ηλεκτρονιακής δόμησης, εντούτοις παραμένουν αδιευκρίνιστα ορισμένα σημεία
Στο παράδειγμα του Fe, δεν ξέρουμε πως ακριβώς κατανέμονται τα 6 ηλεκτρόνια στα 3d τροχιακά.
Γνωρίζουμε ότι η συνολική χωρητικότητα των 3d είναι 10 ηλεκτρόνια, αλλά δεν γνωρίζουμε αν μένει ή όχι κάποιο d τροχιακό κενό.
Την απάντηση σ' αυτού του είδους τα ερωτήματα δίνει ο κανόνας του Hund από τον οποίο προκύπτει:
> «Ηλεκτρόνια που καταλαμβάνουν τροχιακά της ίδιας ενέργειας (της ίδιας υποστιβάδας) έχουν κατά προτίμηση παράλληλα spin».
Για παράδειγμα στο άτομο του αζώτου 7Ν η κατανομή σε υποστιβάδες είναι:
ή αναλυτικότερα, αν θέλουμε να δείξουμε την κατανομή των ηλεκτρονίων στα τροχιακά:
Παρακολουθήστε τα κινούμενα σχέδια που έχουν σχέση με την ηλεκτρονιακή δόμηση πολυηλεκτρονιακών ατόμων.Πατήστε το κουμπί electron configuration και δείτε την δόμηση των πολυηλεκτρονιακών ατόμων. Κατόπιν με κάθε πάτημα του ποντικιού πάμε στο άτομο στην θεμελιώδη κατάσταση με ατομικό αριθμό +1 σε σχέση με το προηγούμενο.
Παρατηρήστε αν στο άτομο του Υδρογόνου οι διάφορες υποστιβάδες τις ίδιας στιβάδας έχουν την ίδια ενέργεια;
Στα επόμενα άτομα ισχύει αυτό;
Προσπαθήστε να εξηγήσετε τις παρατηρήσεις σας με βάση τις προηγούμενες γνώσεις σας.
Με ποιους κβαντικούς αριθμούς καθορίζεται η ενέργεια της κάθε υποστιβάδας 1) στο άτομο του υδρογόνου
2) στα πολυηλεκτρονιακα άτομα;
Ακολουθώντας τις οδηγίες στα αγγλικά, παίξτε το διαδικτυακό παιχνίδι και ελέγξτε τις γνώσεις σας πάνω στη τροχιακά.
Στην αρχή στα 3 τετραγωνάκια τοποθετήστε μια έγκυρη ηλεκτρονιακή δομή της μορφής π.χ 4d 3. Κατόπιν πατήστε το κουμπί Submit με σκοπό να επιβεβαιώσετε ότι αυτή η δομή υπάρχει.
Κατόπιν εάν υπάρχει πατήστε το κουμπί advance to quantum numbers. Πριν πατήσετε το generate n σκεφτείτε ποιος είναι ο κύριος κβαντικός αριθμός. Επιβεβαιώστε την υπόθεσή σας με το πάτημα του κουμπιού.
Κατόπιν σκεφτείτε ποια τιμή πρέπει να παίρνει ο δευτερεύων κβαντικός αριθμός και συνεχίστε την διαδικασία επιλέγοντας μέσω του κουτιού choose.
Κατόπιν εμφανίζονται οι πιθανές διατάξεις των ηλεκτρονίων μέσα στα τροχιακά. πια τιμή ml θα επιλέξω την επιλέγω μέσω της εντολή choose αντιστοιχώντας την με την θέση που εμφανίζεται στην παραπάνω εικόνα. Οι αρνητικές τιμές αντιστοιχούν στα αριστερά των σχημάτων και η μεγαλύτερη θετική στα δεξιά.
Τέλος επιλέγουμε το συνολικό άθροισμα του σπιν των ηλεκτρονίων, αν είναι θετικό ή αρνητικό.
Αφού τελειώσετε με την γνωριμία του λογισμικού προχωρήστε στις παρακάτω ενέργειες. Καταγράψτε σε ένα φύλλο χαρτί τις απαντήσεις σας.
Θέστε τα παρακάτω ηλεκτρονιακές δομές και ελέγξτε εάν υπάρχουν.
3d7
3f11
2p6
2s3
4s1
4p5
4d9
Αιτιολογήστε γιατί κάποιες από αυτές δεν είναι δυνατόν να υπάρχουν.
Σε αυτές τις ηλεκτρονιακές δομές που υπάρχουν, υποθέστε τους κβαντικούς αριθμούς n, l, ml, ms και κατόπιν παίξτε το παραπάνω παιχνίδι για να ελέγξετε τις απαντήσεις σας.
Παρατηρήστε αν στο άτομο του Υδρογόνου οι διάφορες υποστιβάδες τις ίδιας στιβάδας έχουν την ίδια ενέργεια;
Στα επόμενα άτομα ισχύει αυτό;
Προσπαθήστε να εξηγήσετε τις παρατηρήσεις σας με βάση τις προηγούμενες γνώσεις σας.
Με ποιους κβαντικούς αριθμούς καθορίζεται η ενέργεια της κάθε υποστιβάδας 1) στο άτομο του υδρογόνου
2) στα πολυηλεκτρονιακα άτομα;
Ακολουθώντας τις οδηγίες στα αγγλικά, παίξτε το διαδικτυακό παιχνίδι και ελέγξτε τις γνώσεις σας πάνω στη τροχιακά.
Στην αρχή στα 3 τετραγωνάκια τοποθετήστε μια έγκυρη ηλεκτρονιακή δομή της μορφής π.χ 4d 3. Κατόπιν πατήστε το κουμπί Submit με σκοπό να επιβεβαιώσετε ότι αυτή η δομή υπάρχει.
Κατόπιν εάν υπάρχει πατήστε το κουμπί advance to quantum numbers. Πριν πατήσετε το generate n σκεφτείτε ποιος είναι ο κύριος κβαντικός αριθμός. Επιβεβαιώστε την υπόθεσή σας με το πάτημα του κουμπιού.
Κατόπιν σκεφτείτε ποια τιμή πρέπει να παίρνει ο δευτερεύων κβαντικός αριθμός και συνεχίστε την διαδικασία επιλέγοντας μέσω του κουτιού choose.
Κατόπιν εμφανίζονται οι πιθανές διατάξεις των ηλεκτρονίων μέσα στα τροχιακά. πια τιμή ml θα επιλέξω την επιλέγω μέσω της εντολή choose αντιστοιχώντας την με την θέση που εμφανίζεται στην παραπάνω εικόνα. Οι αρνητικές τιμές αντιστοιχούν στα αριστερά των σχημάτων και η μεγαλύτερη θετική στα δεξιά.
Τέλος επιλέγουμε το συνολικό άθροισμα του σπιν των ηλεκτρονίων, αν είναι θετικό ή αρνητικό.
Αφού τελειώσετε με την γνωριμία του λογισμικού προχωρήστε στις παρακάτω ενέργειες. Καταγράψτε σε ένα φύλλο χαρτί τις απαντήσεις σας.
Θέστε τα παρακάτω ηλεκτρονιακές δομές και ελέγξτε εάν υπάρχουν.
3d7
3f11
2p6
2s3
4s1
4p5
4d9
Αιτιολογήστε γιατί κάποιες από αυτές δεν είναι δυνατόν να υπάρχουν.
Σε αυτές τις ηλεκτρονιακές δομές που υπάρχουν, υποθέστε τους κβαντικούς αριθμούς n, l, ml, ms και κατόπιν παίξτε το παραπάνω παιχνίδι για να ελέγξετε τις απαντήσεις σας.
Παρακολουθήστε τα παρακάτω βίντεο που θα σας βοηθήσουν στην κατανόηση της διαδικασίας της ηλεκτρονιακής δόμησης των πολυηλεκτρονιακών ατόμων
Για να ελέγξετε τις γνώσεις σας απαντήστε τις ερωτήσεις στο παρακάτω αρχείο
| polyhlektroniaka_atoma.docx | |
| File Size: | 117 kb |
| File Type: | docx |