H θεωρία του Bohr, παρά τη μεγάλη επιτυχία που γνώρισε στην αρχή, έπρεπε να εγκαταλειφθεί δώδεκα μόλις χρόνια μετά, καθώς δεν κατάφερε να ερμηνεύσει, ούτε τα φάσματα εκπομπής πολυπλοκότερων του υδρογόνου ατόμων (πολυηλεκτρονικά άτομα π.χ. He, Li κλπ.), ούτε το χημικό δεσμό.
Τη βάση για την ανάπτυξή των σύγχρονων αντιλήψεων γύρω από το άτομο έδωσε η κυματική Θεωρία της ύλης του De Broglie (1924):
> To φως, του οποίου το κβάντο ονομάζεται φωτόνιο, όπως και κάθε κινούμενο μικρό σωματίδιο π.χ. ηλεκτρόνιο, παρουσιάζει διττή φύση, σωματιδίου (κβάντα) και κύματος (ηλεκτρομαγνητικό κύμα) .
Δείτε το παρακάτω βίντεο κε το πείραμα των δύο σχισμών με σκοπό να διαπιστώσετε την διπλή φύση του φωτός
Τη βάση για την ανάπτυξή των σύγχρονων αντιλήψεων γύρω από το άτομο έδωσε η κυματική Θεωρία της ύλης του De Broglie (1924):
> To φως, του οποίου το κβάντο ονομάζεται φωτόνιο, όπως και κάθε κινούμενο μικρό σωματίδιο π.χ. ηλεκτρόνιο, παρουσιάζει διττή φύση, σωματιδίου (κβάντα) και κύματος (ηλεκτρομαγνητικό κύμα) .
Δείτε το παρακάτω βίντεο κε το πείραμα των δύο σχισμών με σκοπό να διαπιστώσετε την διπλή φύση του φωτός

Βέβαια θα πρέπει να διευκρινίσουμε, ότι η φύση του φωτός (ή ηλεκτρονίου) είναι μία, δηλαδή, δεν αλλάζει συνεχώς, απλώς, άλλοτε εκδηλώνεται ο σωματιδιακός και άλλοτε ο κυματικός χαρακτήρας του, ανάλογα με τις πειραματικές συνθήκες που εφαρμόζουμε.
Για παράδειγμα η κυματική φύση των ηλεκτρονίων εκδηλώνεται με την περίθλαση των ηλεκτρονίων σε κρυσταλλικό πλέγμα, η οποία βρίσκει εφαρμογή στη λειτουργία των ηλεκτρονικών μικροσκοπίων.
To μήκος κύματος, λ, ενός σωματιδίου μάζας, m, και ταχύτητας, u, δίνεται από τη σχέση:
λ= h/mu
Από την παραπάνω σχέση προκύπτει ότι για να εκδηλωθεί ο κυματικός χαρακτήρας ενός σωματιδίου θα πρέπει αυτό να έχει μικρή μάζα και μεγάλη ταχύτητα.
Π.χ. μπάλα του τένις, κινούμενη με ταχύτητα 65 km h-1 αντιστοιχεί σε υλικό μήκους κύματος λ < 10-33 m, το οποίο υπολείπεται κατά πολύ ακόμη και της διαμέτρου των ατομικών πυρήνων.
Αντίθετα, η πολύ μικρή μάζα και η σχετικά μεγάλη ταχύτητα των ηλεκτρονίων μας επιτρέπουν να ανιχνεύσουμε την κυματική φύση της κίνησης τους (λ ~ 10-10 m).
Θεμελιώδης επίσης συμβολή στην ανάπτυξη της σύγχρονης αντίληψης για το άτομο έδωσε η αρχή της αβεβαιότητας (απροσδιοριστίας) του Heisenberg (1927):
> Είναι αδύνατο να προσδιορίσουμε με ακρίβεια συγχρόνως τη θέση και την ορμή (p= m u) ενός μικρού σωματιδίου π.χ. ηλεκτρονίου.
Δηλαδή, όσο μεγαλύτερη είναι η ακρίβεια για τον προσδιορισμό της θέσης του σωματιδίου (π.χ. ηλεκτρονίου), τόσο μεγαλύτερο είναι το σφάλμα, δηλαδή, τόσο μεγαλύτερη αβεβαιότητα υπάρχει κατά τον προσδιορισμό της ορμής του, και αντιστρόφως.
Στην περίπτωση μεγάλων σωμάτων, π.χ. κινούμενη μπάλα ποδοσφαίρου, τα σφάλματα αυτά είναι αμελητέα. Έτσι, μπορεί να προσδιοριστεί με ακρίβεια ταυτόχρονα η θέση και η ταχύτητα της μπάλας, οποιαδήποτε χρονική στιγμή.
Στην περίπτωση, όμως, υποατομικών σωματιδίων π.χ. ηλεκτρονίων τα σφάλματα αυτά δεν μπορούν να θεωρηθούν αμελητέα και κατά συνέπεια υπάρχει πάντοτε κάποια αβεβαιότητα, είτε ως προς τη θέση, είτε ως προς την ορμή τους.
H αποδοχή της αρχής της αβεβαιότητας οδηγεί αυτομάτως στην κατάρριψη όλων των πλανητικών προτύπων, συμπεριλαμβανομένου και του ατομικού πρότυπου Bohr. Πράγματι η παραδοχή της κίνησης του ηλεκτρονίου σε καθορισμένη κυκλική τροχιά προϋποθέτει, με βάση τους νόμους της κυκλικής κίνησης, επακριβή γνώση της θέσης και της ταχύτητας
Την ίδια εποχή ο Schrodinger έδωσε την περίφημη κυματική εξίσωση, η οποία μαθηματικά συσχετίζει τη σωματιδιακή και κυματική συμπεριφορά του ηλεκτρονίου.
Εδώ ανοίγει ο δρόμος για την ανάπτυξη της κβαντομηχανικής, μιας νέας μηχανικής που μπορεί να εφαρμοστεί στο μικρόκοσμο του ατόμου.
Σήμερα δε θεωρούμε πλέον ότι ένα ηλεκτρόνιο κινείται σε μια ορισμένη τροχιά γύρω από τον πυρήνα. Στην κβαντομηχανική δε μιλάμε για τη θέση ενός ηλεκτρονίου, αλλά για την πιθανότητα να βρίσκεται σε μια ορισμένη θέση ένα ηλεκτρόνιο.
Με βάση την εξίσωση Schrodinger υπολογίζεται η ενέργεια, En, του ηλεκτρονίου, η οποία βρίσκεται σε πλήρη ταύτιση με αυτή που προσδιόρισε ο Bohr (κβάντωση ενέργειας).
Επιπλέον η εξίσωση προσδιορίζει την πιθανότητα εύρεσης του ηλεκτρονίου σε ορισμένο χώρο, πράγμα που βρίσκεται σε πλήρη αντίθεση με τις αντιλήψεις του Bohr (καθορισμένες τροχιές). Πιο αναλυτικά, η επίλυση της εξίσωσης Schrodinger οδηγεί στις κυματοσυναρτήσεις ψ, οι οποίες περιγράφουν την κατάσταση του ηλεκτρονίου με ορισμένη ενέργεια (En) και ονομάζονται ατομικά τροχιακά. H ονομασία αυτή δόθηκε για να τιμηθεί η προσφορά του Bohr.
Τα ατομικά τροχιακά αποτελούν συναρτήσεις θέσης του ηλεκτρονίου στο άτομο π.χ. είναι της μορφής ψ(x, y, z), όπου x, y, z είναι οι συντεταγμένες που καθορίζουν τη θέση του ηλεκτρονίου γύρω από τον πυρήνα. To ψ αυτό καθεαυτό δεν έχει φυσική σημασία. Βέβαια, αποτελεί κατά κάποιο τρόπο μια ένδειξη της παρουσίας, ή μη, του ηλεκτρονίου γύρω από τον πυρήνα (ψ =0 υποδηλώνει την απουσία και ψ#0 την παρουσία του ηλεκτρονίου). Αντίθετα, το ψ2 έχει σημαντική φυσική σημασία, καθώς
> To ψ2 εκφράζει την πιθανότητα να βρεθεί το ηλεκτρόνιο σε ένα ορισμένο σημείο του χώρου γύρω από τον πυρήνα.
Για παράδειγμα:
Στη θέση A: ψ= 0,1 ή ψ2 = 0,01
Στη θέση B: ψ = -0,3 ή ψ2 = 0,09
Δηλαδή, η πιθανότητα να βρίσκεται το ηλεκτρόνιο στη θέση B είναι εννιά φορές μεγαλύτερη από όσο στη θέση Α.
Με άλλα λόγια μπορούμε να πούμε ότι,
> To ψ2 (ή ακριβέστερα το -eψ2, όπου -e το φορτίο του ηλεκτρονίου) εκφράζει την κατανομή ή την πυκνότητα του ηλεκτρονιακού νέφους στο χώρο γύρω από τον πυρήνα.
Εδώ θα πρέπει να παρατηρήσουμε, ότι η εξίσωση Schrodinger διατυπώθηκε για να περιγράψει μαθηματικά τη συμπεριφορά του ηλεκτρονίου του ατόμου του υδρογόνου. Μπορεί βέβαια με κατάλληλες προσεγγίσεις να εφαρμοστεί και σε πολυηλεκτρονικά άτομα, παρόλο που η επίλυση της εξίσωσης και ο προσδιορισμός των κυματοσυναρτήσεων, ψ, για τα ηλεκτρόνια σ' αυτές τις περιπτώσεις είναι ένα πολύπλοκο μαθηματικό πρόβλημα. Ωστόσο, τα συμπεράσματα που προκύπτουν από το υδρογόνο, μπορούν να αποτελέσουν τη βάση για να μελετήσουμε την ηλεκτρονιακή δομή βαρύτερων ατόμων.
Παρακάτω δίνεται υπό μορφή παραδείγματος, η σχηματική απεικόνιση του ηλεκτρονιακού νέφους (της συνάρτησης ψ2) του ατόμου του υδρογόνου, στη θεμελιώδη του κατάσταση
Για παράδειγμα η κυματική φύση των ηλεκτρονίων εκδηλώνεται με την περίθλαση των ηλεκτρονίων σε κρυσταλλικό πλέγμα, η οποία βρίσκει εφαρμογή στη λειτουργία των ηλεκτρονικών μικροσκοπίων.
To μήκος κύματος, λ, ενός σωματιδίου μάζας, m, και ταχύτητας, u, δίνεται από τη σχέση:
λ= h/mu
Από την παραπάνω σχέση προκύπτει ότι για να εκδηλωθεί ο κυματικός χαρακτήρας ενός σωματιδίου θα πρέπει αυτό να έχει μικρή μάζα και μεγάλη ταχύτητα.
Π.χ. μπάλα του τένις, κινούμενη με ταχύτητα 65 km h-1 αντιστοιχεί σε υλικό μήκους κύματος λ < 10-33 m, το οποίο υπολείπεται κατά πολύ ακόμη και της διαμέτρου των ατομικών πυρήνων.
Αντίθετα, η πολύ μικρή μάζα και η σχετικά μεγάλη ταχύτητα των ηλεκτρονίων μας επιτρέπουν να ανιχνεύσουμε την κυματική φύση της κίνησης τους (λ ~ 10-10 m).
Θεμελιώδης επίσης συμβολή στην ανάπτυξη της σύγχρονης αντίληψης για το άτομο έδωσε η αρχή της αβεβαιότητας (απροσδιοριστίας) του Heisenberg (1927):
> Είναι αδύνατο να προσδιορίσουμε με ακρίβεια συγχρόνως τη θέση και την ορμή (p= m u) ενός μικρού σωματιδίου π.χ. ηλεκτρονίου.
Δηλαδή, όσο μεγαλύτερη είναι η ακρίβεια για τον προσδιορισμό της θέσης του σωματιδίου (π.χ. ηλεκτρονίου), τόσο μεγαλύτερο είναι το σφάλμα, δηλαδή, τόσο μεγαλύτερη αβεβαιότητα υπάρχει κατά τον προσδιορισμό της ορμής του, και αντιστρόφως.
Στην περίπτωση μεγάλων σωμάτων, π.χ. κινούμενη μπάλα ποδοσφαίρου, τα σφάλματα αυτά είναι αμελητέα. Έτσι, μπορεί να προσδιοριστεί με ακρίβεια ταυτόχρονα η θέση και η ταχύτητα της μπάλας, οποιαδήποτε χρονική στιγμή.
Στην περίπτωση, όμως, υποατομικών σωματιδίων π.χ. ηλεκτρονίων τα σφάλματα αυτά δεν μπορούν να θεωρηθούν αμελητέα και κατά συνέπεια υπάρχει πάντοτε κάποια αβεβαιότητα, είτε ως προς τη θέση, είτε ως προς την ορμή τους.
H αποδοχή της αρχής της αβεβαιότητας οδηγεί αυτομάτως στην κατάρριψη όλων των πλανητικών προτύπων, συμπεριλαμβανομένου και του ατομικού πρότυπου Bohr. Πράγματι η παραδοχή της κίνησης του ηλεκτρονίου σε καθορισμένη κυκλική τροχιά προϋποθέτει, με βάση τους νόμους της κυκλικής κίνησης, επακριβή γνώση της θέσης και της ταχύτητας
Την ίδια εποχή ο Schrodinger έδωσε την περίφημη κυματική εξίσωση, η οποία μαθηματικά συσχετίζει τη σωματιδιακή και κυματική συμπεριφορά του ηλεκτρονίου.
Εδώ ανοίγει ο δρόμος για την ανάπτυξη της κβαντομηχανικής, μιας νέας μηχανικής που μπορεί να εφαρμοστεί στο μικρόκοσμο του ατόμου.
Σήμερα δε θεωρούμε πλέον ότι ένα ηλεκτρόνιο κινείται σε μια ορισμένη τροχιά γύρω από τον πυρήνα. Στην κβαντομηχανική δε μιλάμε για τη θέση ενός ηλεκτρονίου, αλλά για την πιθανότητα να βρίσκεται σε μια ορισμένη θέση ένα ηλεκτρόνιο.
Με βάση την εξίσωση Schrodinger υπολογίζεται η ενέργεια, En, του ηλεκτρονίου, η οποία βρίσκεται σε πλήρη ταύτιση με αυτή που προσδιόρισε ο Bohr (κβάντωση ενέργειας).
Επιπλέον η εξίσωση προσδιορίζει την πιθανότητα εύρεσης του ηλεκτρονίου σε ορισμένο χώρο, πράγμα που βρίσκεται σε πλήρη αντίθεση με τις αντιλήψεις του Bohr (καθορισμένες τροχιές). Πιο αναλυτικά, η επίλυση της εξίσωσης Schrodinger οδηγεί στις κυματοσυναρτήσεις ψ, οι οποίες περιγράφουν την κατάσταση του ηλεκτρονίου με ορισμένη ενέργεια (En) και ονομάζονται ατομικά τροχιακά. H ονομασία αυτή δόθηκε για να τιμηθεί η προσφορά του Bohr.
Τα ατομικά τροχιακά αποτελούν συναρτήσεις θέσης του ηλεκτρονίου στο άτομο π.χ. είναι της μορφής ψ(x, y, z), όπου x, y, z είναι οι συντεταγμένες που καθορίζουν τη θέση του ηλεκτρονίου γύρω από τον πυρήνα. To ψ αυτό καθεαυτό δεν έχει φυσική σημασία. Βέβαια, αποτελεί κατά κάποιο τρόπο μια ένδειξη της παρουσίας, ή μη, του ηλεκτρονίου γύρω από τον πυρήνα (ψ =0 υποδηλώνει την απουσία και ψ#0 την παρουσία του ηλεκτρονίου). Αντίθετα, το ψ2 έχει σημαντική φυσική σημασία, καθώς
> To ψ2 εκφράζει την πιθανότητα να βρεθεί το ηλεκτρόνιο σε ένα ορισμένο σημείο του χώρου γύρω από τον πυρήνα.
Για παράδειγμα:
Στη θέση A: ψ= 0,1 ή ψ2 = 0,01
Στη θέση B: ψ = -0,3 ή ψ2 = 0,09
Δηλαδή, η πιθανότητα να βρίσκεται το ηλεκτρόνιο στη θέση B είναι εννιά φορές μεγαλύτερη από όσο στη θέση Α.
Με άλλα λόγια μπορούμε να πούμε ότι,
> To ψ2 (ή ακριβέστερα το -eψ2, όπου -e το φορτίο του ηλεκτρονίου) εκφράζει την κατανομή ή την πυκνότητα του ηλεκτρονιακού νέφους στο χώρο γύρω από τον πυρήνα.
Εδώ θα πρέπει να παρατηρήσουμε, ότι η εξίσωση Schrodinger διατυπώθηκε για να περιγράψει μαθηματικά τη συμπεριφορά του ηλεκτρονίου του ατόμου του υδρογόνου. Μπορεί βέβαια με κατάλληλες προσεγγίσεις να εφαρμοστεί και σε πολυηλεκτρονικά άτομα, παρόλο που η επίλυση της εξίσωσης και ο προσδιορισμός των κυματοσυναρτήσεων, ψ, για τα ηλεκτρόνια σ' αυτές τις περιπτώσεις είναι ένα πολύπλοκο μαθηματικό πρόβλημα. Ωστόσο, τα συμπεράσματα που προκύπτουν από το υδρογόνο, μπορούν να αποτελέσουν τη βάση για να μελετήσουμε την ηλεκτρονιακή δομή βαρύτερων ατόμων.
Παρακάτω δίνεται υπό μορφή παραδείγματος, η σχηματική απεικόνιση του ηλεκτρονιακού νέφους (της συνάρτησης ψ2) του ατόμου του υδρογόνου, στη θεμελιώδη του κατάσταση
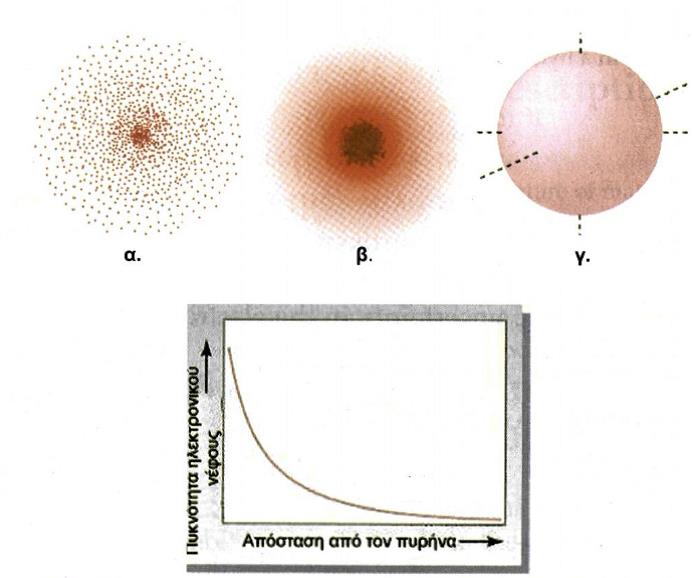
Στην παρουσίαση με «στιγμές» (βλέπε σχήμα α.) η πυκνότητα του ηλεκτρονικού νέφους, που είναι και ανάλογη της πιθανότητας παρουσίας του ηλεκτρονίου, καθορίζεται από τον αριθμό των κουκκίδων ανά μονάδα όγκου. H παράσταση αυτή μας θυμίζει την εικόνα εντόμων γύρω από ένα λαμπτήρα.
Στο β' σχήμα, η πυκνότητα του ηλεκτρονιακού νέφους είναι ανάλογη της πυκνότητας του χρώματος. Να παρατηρήσουμε, ότι το ηλεκτρονιακό νέφος έχει τη μεγίστη πυκνότητα κοντά στον πυρήνα, χωρίς όμως αυτό να σημαίνει ότι εκεί γίνεται εξουδετέρωση φορτίων.
Στις «οριακές» καμπύλες, που είναι και η πιο συνηθισμένη απεικόνιση της πυκνότητας του ηλεκτρονιακού νέφους (ψ2), το περίγραμμα της καμπύλης περικλείει τη μέγιστη πυκνότητα του ηλεκτρονικού νέφους π.χ. 90-99% αυτής.
Τέλος, ξεκαθαρίσουμε ότι οι παραπάνω γραφικές παραστάσεις απεικονίζουν την πυκνότητα του ηλεκτρονιακού νέφους (ψ2) και όχι το τροχιακό (ψ), όπως πολλές φορές αναφέρεται (χάριν απλούστευσης).
Δείτε το παρακάτω βίντεο και κατόπιν απαντήστε τις ερωτήσεις που βρίσκονται στο αρχειο
Στο β' σχήμα, η πυκνότητα του ηλεκτρονιακού νέφους είναι ανάλογη της πυκνότητας του χρώματος. Να παρατηρήσουμε, ότι το ηλεκτρονιακό νέφος έχει τη μεγίστη πυκνότητα κοντά στον πυρήνα, χωρίς όμως αυτό να σημαίνει ότι εκεί γίνεται εξουδετέρωση φορτίων.
Στις «οριακές» καμπύλες, που είναι και η πιο συνηθισμένη απεικόνιση της πυκνότητας του ηλεκτρονιακού νέφους (ψ2), το περίγραμμα της καμπύλης περικλείει τη μέγιστη πυκνότητα του ηλεκτρονικού νέφους π.χ. 90-99% αυτής.
Τέλος, ξεκαθαρίσουμε ότι οι παραπάνω γραφικές παραστάσεις απεικονίζουν την πυκνότητα του ηλεκτρονιακού νέφους (ψ2) και όχι το τροχιακό (ψ), όπως πολλές φορές αναφέρεται (χάριν απλούστευσης).
Δείτε το παρακάτω βίντεο και κατόπιν απαντήστε τις ερωτήσεις που βρίσκονται στο αρχειο
| kbanomhxaniki_eikona_tou_atomou.docx | |
| File Size: | 211 kb |
| File Type: | docx |