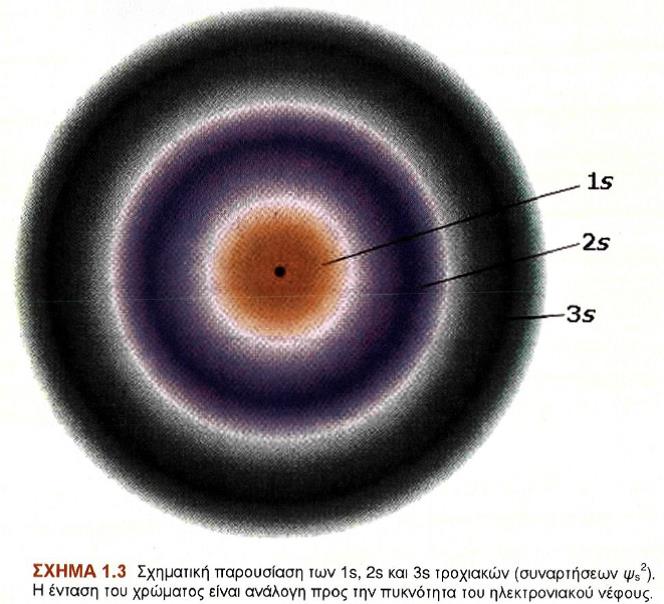
Όπως ήδη έχουμε αναφέρει, η απεικόνιση των ατομικών τροχιακών ή ακριβέστερα της πυκνότητας του ηλεκτρονιακού νέφους μπορεί να γίνει με πολλούς τρόπους. H παράσταση των τροχιακών (συναρτήσεων ψ2) με οριακές καμπύλες είναι από τις πιο συνηθισμένες. Να θυμίσουμε, ότι το περίγραμμα της καμπύλης περικλείει το 90-99% της πυκνότητας του ηλεκτρονιακού νέφους.
Τα s τροχιακά (l = 0) έχουν σφαιρική συμμετρία, που σημαίνει ότι η πιθανότητα να βρεθεί το ηλεκτρόνιο σε μια ορισμένη απόσταση από τον πυρήνα είναι ανεξάρτητη από την κατεύθυνση. Τα s τροχιακά συμβολίζονται με σφαίρες, το μέγεθος των οποίων εξαρτάται από τον κύριο κβαντικό αριθμό. Όσο μεγαλύτερος είναι ο κύριος κβαντικός αριθμός n, στον οποίο ανήκει το τροχιακό s, τόσο μεγαλύτερη είναι και η ακτίνα της σφαίρας
Τα s τροχιακά (l = 0) έχουν σφαιρική συμμετρία, που σημαίνει ότι η πιθανότητα να βρεθεί το ηλεκτρόνιο σε μια ορισμένη απόσταση από τον πυρήνα είναι ανεξάρτητη από την κατεύθυνση. Τα s τροχιακά συμβολίζονται με σφαίρες, το μέγεθος των οποίων εξαρτάται από τον κύριο κβαντικό αριθμό. Όσο μεγαλύτερος είναι ο κύριος κβαντικός αριθμός n, στον οποίο ανήκει το τροχιακό s, τόσο μεγαλύτερη είναι και η ακτίνα της σφαίρας
Με ανάλογη σκέψη, τα p τροχιακά έχουν το σχήμα διπλού λοβού, όπως φαίνεται στο σχήμα 1.4. To σχήμα του λοβού είναι το σχήμα που προκύπτει αν ένα σφαιρικό μπαλόνι «τραβηχτεί» από κάποιο σημείο του, π.χ. από εκεί που είναι δεμένο.
Να παρατηρήσουμε επίσης ότι το ηλεκτρόνιο στο p τροχιακό, αντίθετα από ότι συμβαίνει στο s, έχει ελάχιστη πιθανότητα να βρεθεί κοντά στον πυρήνα.
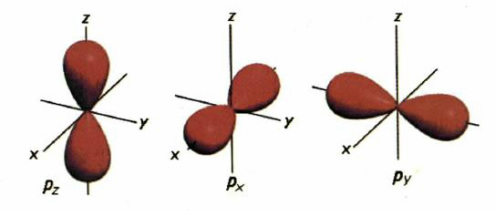
Όπως γνωρίζουμε, σε κάθε τιμή του κύριου κβαντικού αριθμού με αντιστοιχούν τρία p τροχιακά, που έχουν ίδιο μέγεθος και σχήμα αλλά διαφορετικό προσανατολισμό. To καθένα απ' αυτά τα τροχιακά, px, py και pz, προσανατολίζεται στον αντίστοιχο άξονα, x, y και z, όπως φαίνεται στο σχήμα 1.4. Επίσης, όπως και στην περίπτωση των s, το μεγεθος του p τροχιακού καθορίζεται από την τιμή του κύριου κβαντικού αριθμού. Δηλαδή, όσο μεγαλύτερος είναι ο κύριος κβαντικός αριθμός n στον οποίο ανήκει το τροχιακό p, τόσο μεγαλύτερο είναι το μέγεθος του τροχιακού.
Να παρατηρήσουμε επίσης ότι το ηλεκτρόνιο στο p τροχιακό, αντίθετα από ότι συμβαίνει στο s, έχει ελάχιστη πιθανότητα να βρεθεί κοντά στον πυρήνα.
Όπως γνωρίζουμε, σε κάθε τιμή του κύριου κβαντικού αριθμού με αντιστοιχούν τρία p τροχιακά, που έχουν ίδιο μέγεθος και σχήμα αλλά διαφορετικό προσανατολισμό. To καθένα απ' αυτά τα τροχιακά, px, py και pz, προσανατολίζεται στον αντίστοιχο άξονα, x, y και z, όπως φαίνεται στο σχήμα 1.4. Επίσης, όπως και στην περίπτωση των s, το μεγεθος του p τροχιακού καθορίζεται από την τιμή του κύριου κβαντικού αριθμού. Δηλαδή, όσο μεγαλύτερος είναι ο κύριος κβαντικός αριθμός n στον οποίο ανήκει το τροχιακό p, τόσο μεγαλύτερο είναι το μέγεθος του τροχιακού.
ΣΧΗΜΑ 1.4. Σχηματική αναπαράσταση των τριών p τροχιακών, px, py, pz (Συναρτήσεων Ψp2)
Τέλος, τα d τροχιακά (l = 2) είναι πέντε (wl: -2, -1, 0, +1, +2) με σχετικά πολύπλοκη απεικόνιση, που ξεφεύγει από τα όρια διδασκαλίας του παρόντος βιβλίου. To ίδιο ισχύει και για τα f τροχιακά (l = 3) που είναι συνολικά 7 (ml: -3, -2, -2, 0, +1, +2, +3).
Επιλέξτε στον παρακάτω σύνδεσμο το δευτερέυοντα ατομικό αριθμό l και βάλτε τιμές μόνο 0 και 1 με σκοπό να δείτε τα τροχιακά s και p αντίστοιχα. Στο l=0 πόσα τροχιακά παρατηρείτε; Έχει συγκεκτιμμένη κατεύθυνση. Στο l=1 πόσα τροχιακά παρατηρείτε; Τι κατεύθυνση έχει το κάθε τροχιακό. Κατόπιν βάλτε στο l την τιμή 2 και παρατηρείστε τον αριθμό των ατομικών τροχιακών. Το ίδιο κάντε και για l = 3. Το σχήμα των τροχιακών και η κατεύθυνση ξεπερνά τα όρια του σχολικού βιβλίου
Στον παρακάτω σύνδεσμο επιλέξτε τα τροχιακά s, p, d, f αντίστοιχα. Παρατηρείστε το σχήμα του τροχιακού s και κατόπιν του p. Στα p τροχιακά σας δίνεται η δυνατότητα να τα επιλέξετε και τα 3 μαζί. Τα 3p είναι ισοδύναμα ενεργειακά είτε στο άτομο του υδρογόνου είτε και στα πολυηλεκτρονιακά άτομα.
Παρακολουθήστε τα παρακάτω βίντεο
Το πρώτο βίντεο δείχνει τα σχήματα των ατομικών τροχιακών κατά αυξανόμενη ενέργεια.
Το δεύτερο μας δείχνει ότι το ηλεκτρόνιο του ατόμου του υδρογόνου μπορεί να βρεθεί σε άλλο τροχιακό μόνο μετά την απορόφηση κατάλληλης ποσότητας ενέργειας. Εξηγούνται επίσης και οι φασματικές γραμμές απορρόφησης και εκπομπής του ατόμου του υδρογόνου.
Επιλέξτε στον παρακάτω σύνδεσμο το δευτερέυοντα ατομικό αριθμό l και βάλτε τιμές μόνο 0 και 1 με σκοπό να δείτε τα τροχιακά s και p αντίστοιχα. Στο l=0 πόσα τροχιακά παρατηρείτε; Έχει συγκεκτιμμένη κατεύθυνση. Στο l=1 πόσα τροχιακά παρατηρείτε; Τι κατεύθυνση έχει το κάθε τροχιακό. Κατόπιν βάλτε στο l την τιμή 2 και παρατηρείστε τον αριθμό των ατομικών τροχιακών. Το ίδιο κάντε και για l = 3. Το σχήμα των τροχιακών και η κατεύθυνση ξεπερνά τα όρια του σχολικού βιβλίου
Στον παρακάτω σύνδεσμο επιλέξτε τα τροχιακά s, p, d, f αντίστοιχα. Παρατηρείστε το σχήμα του τροχιακού s και κατόπιν του p. Στα p τροχιακά σας δίνεται η δυνατότητα να τα επιλέξετε και τα 3 μαζί. Τα 3p είναι ισοδύναμα ενεργειακά είτε στο άτομο του υδρογόνου είτε και στα πολυηλεκτρονιακά άτομα.
Παρακολουθήστε τα παρακάτω βίντεο
Το πρώτο βίντεο δείχνει τα σχήματα των ατομικών τροχιακών κατά αυξανόμενη ενέργεια.
Το δεύτερο μας δείχνει ότι το ηλεκτρόνιο του ατόμου του υδρογόνου μπορεί να βρεθεί σε άλλο τροχιακό μόνο μετά την απορόφηση κατάλληλης ποσότητας ενέργειας. Εξηγούνται επίσης και οι φασματικές γραμμές απορρόφησης και εκπομπής του ατόμου του υδρογόνου.
Για να κάνετε επανάληψη της θεωρίας των ατομικών τροχιακών διαβάστε την παρακάτω προβολή και απαντήστε στις ερωτήσεις στο παρακάτω αρχείο
| apeikonisi_atomikon_troxiakon.docx | |
| File Size: | 223 kb |
| File Type: | docx |