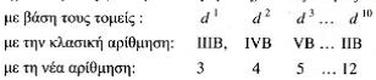Τομείς του περιοδικού πίνακα
Με βάση την ηλεκτρονιακή δομή και συγκεκριμένα τον τύπο της υποστιβάδας στην οποία ανήκει το τελευταίο ηλεκτρόνιο (με τη μεγαλύτερη
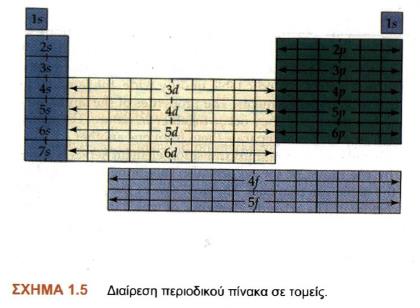
ενέργεια, σύμφωνα με την αρχή ηλεκτρονιακής δόμησης) ο περιοδικός πίνακας μπορεί να διαιρεθεί σε τέσσερις τομείς s, p, d, f, όπως φαίνεται
στο σχήμα 1.5.
Με βάση την ηλεκτρονιακή δομή και συγκεκριμένα τον τύπο της υποστιβάδας στην οποία ανήκει το τελευταίο ηλεκτρόνιο (με τη μεγαλύτερη
ενέργεια, σύμφωνα με την αρχή ηλεκτρονιακής δόμησης) ο περιοδικός πίνακας μπορεί να διαιρεθεί σε τέσσερις τομείς s, p, d, f, όπως φαίνεται
στο σχήμα 1.5.
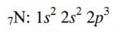
Για παράδειγμα το άζωτο, που έχει την ηλεκτρονιακή δομή
ανήκει στον τομέα p, επειδή το τελευταίο του ηλεκτρόνιο (αυτό με τη μεγαλύτερη ενέργεια) είναι στην υποστιβάδα p.
ανήκει στον τομέα p, επειδή το τελευταίο του ηλεκτρόνιο (αυτό με τη μεγαλύτερη ενέργεια) είναι στην υποστιβάδα p.
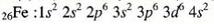
Ανάλογα ο
ανήκει στον τομέα d, επειδή το τελευταίο του ηλεκτρόνιο (με βάση τη σειρά δόμησης aufbau), είναι στην υποστιβάδα d.
Συμπερασματικά μπορούμε να πούμε ότι,
> Τομέας περιοδικού πίνακα είναι ένα σύνολο στοιχείων των οποίων τα άτομα έχουν τα τελευταία τους ηλεκτρόνια (με τη μεγίστη ενέργεια, σύμφωνα με την αρχή ηλεκτρονιακής δόμησης aufbau) στον ίδιο τύπο υποστιβάδας π.χ. s, p, d ή f.
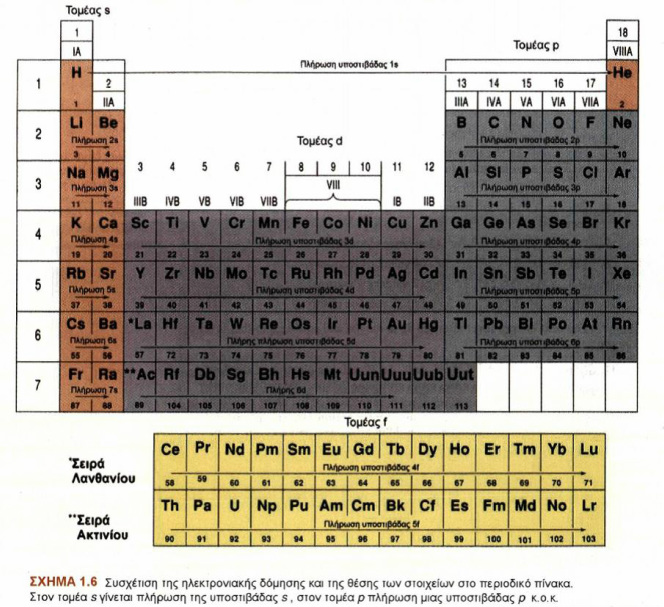
H διαίρεση αυτή του περιοδικού πίνακα σε τομείς δείχνει καθαρά τη σχέση που υπάρχει μεταξύ της ηλεκτρονιακής δομής του ατόμου ενός στοιχείου και της θέσης αυτού στον περιοδικό πίνακα.
Τομέας s: O τομέας s περιλαμβάνει δύο κύριες ομάδες (κατακόρυφες στήλες) του περιοδικού πίνακα Δηλαδή, την ομάδα των αλκαλίων (Na, K κλπ.) και την ομάδα των αλκαλικών γαιών (Ca, Mg κλπ.). Επιπλέον στον τομέα αυτό ανήκει το υδρογόνο. H υποστιβάδα s έχει το πολύ δύο ηλεκτρόνια γι' αυτό και ο τομέας s έχει δύο ομάδες.
Οι ομάδες αυτές ονομάζονται:
ανήκει στον τομέα d, επειδή το τελευταίο του ηλεκτρόνιο (με βάση τη σειρά δόμησης aufbau), είναι στην υποστιβάδα d.
Συμπερασματικά μπορούμε να πούμε ότι,
> Τομέας περιοδικού πίνακα είναι ένα σύνολο στοιχείων των οποίων τα άτομα έχουν τα τελευταία τους ηλεκτρόνια (με τη μεγίστη ενέργεια, σύμφωνα με την αρχή ηλεκτρονιακής δόμησης aufbau) στον ίδιο τύπο υποστιβάδας π.χ. s, p, d ή f.
H διαίρεση αυτή του περιοδικού πίνακα σε τομείς δείχνει καθαρά τη σχέση που υπάρχει μεταξύ της ηλεκτρονιακής δομής του ατόμου ενός στοιχείου και της θέσης αυτού στον περιοδικό πίνακα.
Τομέας s: O τομέας s περιλαμβάνει δύο κύριες ομάδες (κατακόρυφες στήλες) του περιοδικού πίνακα Δηλαδή, την ομάδα των αλκαλίων (Na, K κλπ.) και την ομάδα των αλκαλικών γαιών (Ca, Mg κλπ.). Επιπλέον στον τομέα αυτό ανήκει το υδρογόνο. H υποστιβάδα s έχει το πολύ δύο ηλεκτρόνια γι' αυτό και ο τομέας s έχει δύο ομάδες.
Οι ομάδες αυτές ονομάζονται:
Τομέας p: H υποστιβάδα ρ περιέχει το πολύ έξι ηλεκτρόνια γι' αυτό και ο τομέας p περιλαμβάνει έξι κύριες ομάδες στοιχείων. Οι ομάδες αυτές είναι η ομάδα του βορίου, του άνθρακα, του αζώτου, του θείου, των αλογόνων και των ευγενών αερίων και μπορούν να ονομαστούν:
Τομέας d: O τομέας d περιλαμβάνει στοιχεία των οποίων το τελευταίο ηλεκτρόνιο, κατά την ηλεκτρονιακή δόμηση των ατόμων τους, τοποθετείται σε υποστιβάδα d. O τομέας αυτός περιλαμβάνει τα στοιχεία μετάπτωσης. H υποστιβάδα d χωράει 10 ηλεκτρόνια γι' αυτό και ο τομέας d έχει 10 ομάδες (δευτερεύουσες ομάδες). Αυτές ονομάζονται:
Δηλαδή, το άτομο του σιδήρου ανήκει στον τομέα d, επειδή με βάση την ηλεκτρονιακή δομή (1s2 2S2 2p6 3s2 3p6 3d6 4s2) το τελευταίο του ηλεκτρόνιο βρίσκεται στην υποστιβάδα d. Επίσης μπορούμε να πούμε, ότι ο σίδηρος ανήκει στην ομάδα d 6 ή με βάση τον παλαιό τρόπο αρίθμησης των ομάδων στις τριάδες (VIIIB) ή με το νέο τρόπο αρίθμησης στην 8.
Τομέας f: O τομέας f περιλαμβάνει στοιχεία, των οποίων το τελευταίο ηλεκτρόνιο ανήκει σε υποστιβάδα f. Επειδή η υποστιβάδα/χωράει 14 ηλεκτρόνια, ο τομέας f περιλαμβάνει 14 ομάδες. Στον τομέα αυτό ανήκουν οι λανθανίδες, οι οποίες ανήκουν στην 6η περίοδο και περιλαμβάνουν στοιχεία με ατομικούς αριθμούς 58-71 και οι ακτινίδες, οι οποίες ανήκουν στην 7η περίοδο και περιλαμβάνουν στοιχεία με ατομικούς αριθμούς 90-103.
Τομέας f: O τομέας f περιλαμβάνει στοιχεία, των οποίων το τελευταίο ηλεκτρόνιο ανήκει σε υποστιβάδα f. Επειδή η υποστιβάδα/χωράει 14 ηλεκτρόνια, ο τομέας f περιλαμβάνει 14 ομάδες. Στον τομέα αυτό ανήκουν οι λανθανίδες, οι οποίες ανήκουν στην 6η περίοδο και περιλαμβάνουν στοιχεία με ατομικούς αριθμούς 58-71 και οι ακτινίδες, οι οποίες ανήκουν στην 7η περίοδο και περιλαμβάνουν στοιχεία με ατομικούς αριθμούς 90-103.
Βρείτε τον ατομικό αριθμό, τον αριθμό της ομάδας, της περιόδου, του τομέα και γράψτε την ηλεκτρονιακή δομή των παρακάτω στοιχείων.
Ι) Το 1ο αλογόνο
ΙΙ) Το 3ο στοιχείο του p τομέα της 3ης περιόδου
ΙΙΙ) το 2ο στοιχείο του τομέα s.
IV) το 6ο στοιχείο του τομέα d
V) το στοιχείο που με το οποίο τελειώνει η 3η περίοδος
VI) το 1ο στοιχείο του τομέα f
Καταγράψτε τα αποτελέσματα σας σε ένα χαρτί και χρησιμοποιήστε αυτή την ιστοσελίδα ή αυτή για να ελέγξετε τις απαντήσεις σας.
Στην 1η ιστοσελίδα στην κάτω αριστερή πλευρά πατήστε το electron configuration.
Στην 2η ιστοσελίδα πατήστε πάνω δεξιά εκεί που αναφέρει S P D F για να δείτε τους αντίστοιχους τομείς.
Οι ιστοσελίδες αυτές θα σας χρησιμεύσουν αργότερα και στην μελέτη των ιδιοτήτων των στοιχείων.
Ι) Το 1ο αλογόνο
ΙΙ) Το 3ο στοιχείο του p τομέα της 3ης περιόδου
ΙΙΙ) το 2ο στοιχείο του τομέα s.
IV) το 6ο στοιχείο του τομέα d
V) το στοιχείο που με το οποίο τελειώνει η 3η περίοδος
VI) το 1ο στοιχείο του τομέα f
Καταγράψτε τα αποτελέσματα σας σε ένα χαρτί και χρησιμοποιήστε αυτή την ιστοσελίδα ή αυτή για να ελέγξετε τις απαντήσεις σας.
Στην 1η ιστοσελίδα στην κάτω αριστερή πλευρά πατήστε το electron configuration.
Στην 2η ιστοσελίδα πατήστε πάνω δεξιά εκεί που αναφέρει S P D F για να δείτε τους αντίστοιχους τομείς.
Οι ιστοσελίδες αυτές θα σας χρησιμεύσουν αργότερα και στην μελέτη των ιδιοτήτων των στοιχείων.
Παρακολουθήστε το παρακάτω βίντεο για μία σύντομη επανάληψη πάνω στην δομή και στις ιδιότητες του περιοδικού πίνακα.
Προς το τέλος του βίντεο υπάρχουν κάποιες ερωτήσεις.
Σταματήστε το βίντεο και προσπαθήστε να τις απαντήσετε καταγράφοντας τις απαντήσεις σας σε ένα φύλλο χαρτί.
Στο τέλος του βίντεο υπάρχουν οι απαντήσεις.
Καλή επιτυχία.
Προς το τέλος του βίντεο υπάρχουν κάποιες ερωτήσεις.
Σταματήστε το βίντεο και προσπαθήστε να τις απαντήσετε καταγράφοντας τις απαντήσεις σας σε ένα φύλλο χαρτί.
Στο τέλος του βίντεο υπάρχουν οι απαντήσεις.
Καλή επιτυχία.
Για να ολοκληρώσετε την ιστοαναζήτηση κάντε μια γρήγορη επανάληψη με την παρακάτω προβολή και απαντήστε στις ερωτήσεις που βρίσκονται στο αρχείο στο τέλος της σελίδας.
| periodikos_pinakas.docx | |
| File Size: | 187 kb |
| File Type: | docx |