To 1913 o Δανός φυσικός Niels Bohr πρότεινε ένα ατομικό πρότυπο (ακολουθήστε τον σύνδεσμο για την ιστορική αναδρομή μέσω της προβολής των κινουμένων σχεδίων) το οποίο συνδυάζει την ιδέα του ατομικού προτύπου του Rutherford και την κβαντική θεωρία του Planck.
Tο ατομικό πρότυπο του Bohr, εφαρμόζεται για το άτομο του υδρογόνου ( αποτελείται από ένα πρωτόνιο και ένα ηλεκτρόνιο) και για τα υδρογονοειδή ιόντα ( ιόντα που έχουν ένα ηλεκτρόνια και έναν πυρήνα) π.χ 2Ηe+, 3Li2+ κλπ, μπορεί να περιγραφεί με δύο συνθήκες
Tο ατομικό πρότυπο του Bohr, εφαρμόζεται για το άτομο του υδρογόνου ( αποτελείται από ένα πρωτόνιο και ένα ηλεκτρόνιο) και για τα υδρογονοειδή ιόντα ( ιόντα που έχουν ένα ηλεκτρόνια και έναν πυρήνα) π.χ 2Ηe+, 3Li2+ κλπ, μπορεί να περιγραφεί με δύο συνθήκες
1η συνθήκη (μηχανική συνθήκη)
Το ηλεκτρόνιο κινείται γύρω από τον πυρήνα σε ορισμένες μόνο κυκλικές τροχιές οι οποίες έχουν καθορισμένη απόσταση (ακτίνα r) από τον πυρήνα (επιτρεπόμενες τροχιές). Κάθε επιτρεπόμενη τροχιά έχει καθορισμένη ενέργεια, είναι δηλαδή κβαντισμένη.
Η ολική ενέργεια του ηλεκτρονίου (το άθροισμα της κινητικής και της δυναμικής του ενέργειας) στο άτομο του υδρογόνου δίνεται από τον τύπο: En = - 2.18 10-18/ n2
όπου, n = 1, 2, 3, .. ο κύριος κβαντικός αριθμός, ο οποίος καθορίζει την ενεργειακή στάθμη του ηλεκτρονίου.
To αρνητικό πρόσημο στην παραπάνω έκφραση έχει τη φυσική έννοια ότι όσο μεγαλώνει η τιμή του η, τόσο μεγαλώνει η ενέργεια του ηλεκτρονίου.
Με άλλα λόγια, όσο το ηλεκτρόνιο απομακρύνεται από τον πυρήνα, τόσο μεγαλώνει η ενέργεια του. Αναμένεται μάλιστα να πάρει τη μεγίστη τιμή
(E = 0), όταν το ηλεκτρόνιο απομακρυνθεί αρκετά και η έλξη του πυρήνα μηδενιστεί.
Σ' αυτή την περίπτωση, το ηλεκτρόνιο παύει πλέον να ανήκει στο άτομο και έχει επέλθει ιοντισμός.
Ένα άτομο λέμε ότι είναι σε θεμελιώδη κατάσταση, όταν τα ηλεκτρόνια του είναι κατά το δυνατό πλησιέστερα στον πυρήνα. Αντίθετα, λέμε πως το άτομο είναι σε διέγερση, όταν π.χ. με θέρμανση τα ηλεκτρόνια μεταπηδήσουν σε υψηλότερες ενεργειακές στάθμες.
2η συνθήκη (οπτική συνθήκη)
To ηλεκτρόνιο εκπέμπει ή απορροφά ενέργεια υπό μορφή ακτινοβολίας μόνο όταν μεταπηδά από μια τροχιά σε μια άλλη, όταν δηλαδή αλλάζει ενεργειακή στάθμη.
Ειδικότερα, όταν ένα ηλεκτρόνιο μεταπίπτει από υψηλότερη σε χαμηλότερη ενεργειακή στάθμη τότε εκπέμπει ακτινοβολία, ενώ όταν μεταπίπτει από χαμηλότερη σε υψηλότερη ενεργειακή στάθμη τότε απορροφά ενέργεια.
Σύμφωνα με τις αντιλήψεις του Γερμανού φυσικού Planck (1900) και του Γερμανοεβραίου φυσικού Αλβέρτου Αϊνσταιν (1905) , οι οποίες εγκαινιάζουν μια νέα θεώρηση στην ερμηνεία του μικρόκοσμου (κβαντική θεωρία), έχουμε :
H ακτινοβολία εκπέμπεται όχι με συνεχή τρόπο αλλά σε μικρά πακέτα (κβάντα). Τα κβάντα φωτός ή της ηλεκτρομαγνητικής ακτινοβολίας γενικότερα ονομάζονται φωτόνια.
Με βάση τις σκέψεις του Planck κάθε κβάντο μεταφέρει ενέργεια, Ε, ανάλογη προς τη συχνότητα της εκπεμπόμενης ακτινοβολίας, ν. Δηλαδή, Ε= hv
όπου, h : η σταθερά Planck, που είναι ίση με 6,63 10-34 J s.
Υιοθετώντας τις ιδέες του Planck του Ritz, και του Balmer., ο Bohr οδηγήθηκε στην παρακάτω
εξίσωση:
ΔΕ=[Εf - Ei] = hν
όπου
Εf = Ενέργεια τελική
Ei = Ενέργεια αρχική
η οποία συσχετίζει τη διαφορά ενέργειας ΔΕ, κατά την μετάπτωση ηλεκτρονίου από μια ενεργειακή στάθμη (Ei), σε μια άλλη (Ef), με τη συχνότητα της εκπεμπόμενης ακτινοβολίας, v.
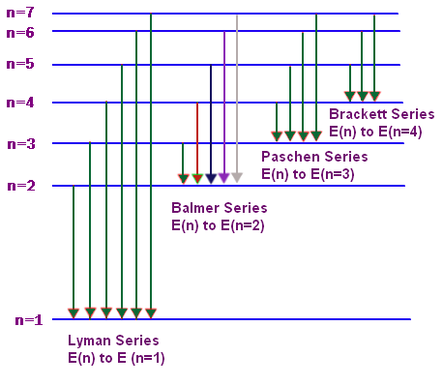
To πρότυπο του Bohr είχε μεγάλη επιτυχία στην ερμηνεία του γραμμικού φάσματος εκπομπής του ατόμου του υδρογόνου.
Κάθε φασματική γραμμή μπορούσε να συσχετιστεί με μεταπτώσεις ηλεκτρονίων προς την ίδια ενεργειακή στάθμη
Για περαιτέρω πληροφορίες σχετικά με τα φάσματα εκπομπής και απορρόφησης ανοίξτε το παρακάτω αρχείο
Το ηλεκτρόνιο κινείται γύρω από τον πυρήνα σε ορισμένες μόνο κυκλικές τροχιές οι οποίες έχουν καθορισμένη απόσταση (ακτίνα r) από τον πυρήνα (επιτρεπόμενες τροχιές). Κάθε επιτρεπόμενη τροχιά έχει καθορισμένη ενέργεια, είναι δηλαδή κβαντισμένη.
Η ολική ενέργεια του ηλεκτρονίου (το άθροισμα της κινητικής και της δυναμικής του ενέργειας) στο άτομο του υδρογόνου δίνεται από τον τύπο: En = - 2.18 10-18/ n2
όπου, n = 1, 2, 3, .. ο κύριος κβαντικός αριθμός, ο οποίος καθορίζει την ενεργειακή στάθμη του ηλεκτρονίου.
To αρνητικό πρόσημο στην παραπάνω έκφραση έχει τη φυσική έννοια ότι όσο μεγαλώνει η τιμή του η, τόσο μεγαλώνει η ενέργεια του ηλεκτρονίου.
Με άλλα λόγια, όσο το ηλεκτρόνιο απομακρύνεται από τον πυρήνα, τόσο μεγαλώνει η ενέργεια του. Αναμένεται μάλιστα να πάρει τη μεγίστη τιμή
(E = 0), όταν το ηλεκτρόνιο απομακρυνθεί αρκετά και η έλξη του πυρήνα μηδενιστεί.
Σ' αυτή την περίπτωση, το ηλεκτρόνιο παύει πλέον να ανήκει στο άτομο και έχει επέλθει ιοντισμός.
Ένα άτομο λέμε ότι είναι σε θεμελιώδη κατάσταση, όταν τα ηλεκτρόνια του είναι κατά το δυνατό πλησιέστερα στον πυρήνα. Αντίθετα, λέμε πως το άτομο είναι σε διέγερση, όταν π.χ. με θέρμανση τα ηλεκτρόνια μεταπηδήσουν σε υψηλότερες ενεργειακές στάθμες.
2η συνθήκη (οπτική συνθήκη)
To ηλεκτρόνιο εκπέμπει ή απορροφά ενέργεια υπό μορφή ακτινοβολίας μόνο όταν μεταπηδά από μια τροχιά σε μια άλλη, όταν δηλαδή αλλάζει ενεργειακή στάθμη.
Ειδικότερα, όταν ένα ηλεκτρόνιο μεταπίπτει από υψηλότερη σε χαμηλότερη ενεργειακή στάθμη τότε εκπέμπει ακτινοβολία, ενώ όταν μεταπίπτει από χαμηλότερη σε υψηλότερη ενεργειακή στάθμη τότε απορροφά ενέργεια.
Σύμφωνα με τις αντιλήψεις του Γερμανού φυσικού Planck (1900) και του Γερμανοεβραίου φυσικού Αλβέρτου Αϊνσταιν (1905) , οι οποίες εγκαινιάζουν μια νέα θεώρηση στην ερμηνεία του μικρόκοσμου (κβαντική θεωρία), έχουμε :
H ακτινοβολία εκπέμπεται όχι με συνεχή τρόπο αλλά σε μικρά πακέτα (κβάντα). Τα κβάντα φωτός ή της ηλεκτρομαγνητικής ακτινοβολίας γενικότερα ονομάζονται φωτόνια.
Με βάση τις σκέψεις του Planck κάθε κβάντο μεταφέρει ενέργεια, Ε, ανάλογη προς τη συχνότητα της εκπεμπόμενης ακτινοβολίας, ν. Δηλαδή, Ε= hv
όπου, h : η σταθερά Planck, που είναι ίση με 6,63 10-34 J s.
Υιοθετώντας τις ιδέες του Planck του Ritz, και του Balmer., ο Bohr οδηγήθηκε στην παρακάτω
εξίσωση:
ΔΕ=[Εf - Ei] = hν
όπου
Εf = Ενέργεια τελική
Ei = Ενέργεια αρχική
η οποία συσχετίζει τη διαφορά ενέργειας ΔΕ, κατά την μετάπτωση ηλεκτρονίου από μια ενεργειακή στάθμη (Ei), σε μια άλλη (Ef), με τη συχνότητα της εκπεμπόμενης ακτινοβολίας, v.
To πρότυπο του Bohr είχε μεγάλη επιτυχία στην ερμηνεία του γραμμικού φάσματος εκπομπής του ατόμου του υδρογόνου.
Κάθε φασματική γραμμή μπορούσε να συσχετιστεί με μεταπτώσεις ηλεκτρονίων προς την ίδια ενεργειακή στάθμη
Για περαιτέρω πληροφορίες σχετικά με τα φάσματα εκπομπής και απορρόφησης ανοίξτε το παρακάτω αρχείο
| _.pdf | |
| File Size: | 1130 kb |
| File Type: | |
θεμελιώδεις και διεγερμένες καταστάσεις στο άτομο του υδρογόνου
Θεμελιώδης κατάσταση ενός ατόμου ονομάζεται η κατάσταση με τη χαμηλότερη ενέργεια . Tο άτομο του υδρογόνου έχει την ελάχιστη ενέργεια όταν το ηλεκτρόνιο κινείται στην πιο κοντινή τροχιά στον πυρήνα δηλαδή όταν το n=1 (στιβάδα Κ), τότε ισχύει
Ε1=-2,18 10-18 j (ελάχιστη ενέργεια)
Διεγερμένη κατάσταση ενός ατόμου ονομάζεται η κατάσταση η οποία έχει υψηλότερη ενέργεια από την θεμελιώδη. στο άτομο του υδρογόνου διεγερμένες καταστάσεις είναι όλες οι ενεργειακές στάθμες που έχουν n>1 δηλαδή Ε2, Ε3 κ.ο.κ (στιβάδες L, M, N ..)
H ενέργεια του ηλεκτρονίου σε μια διεγερμένη κατάσταση μπορεί να εκφραστεί σε συνάρτηση με την ενέργεια του ηλεκτρονίου στη θεμελιώδη κατάσταση Ε1.
Ισχύει Εn= - 2,18 10-18 /n2 όπου n = 2,3,4...
Aν το άτομο του υδρογόνου που βρίσκεται στη θεμελιώδη κατάσταση (n=1) απορροφήσει ενέργεια (για παράδειγμα με απορρόφηση ακτινοβολίας ή με κρούση με άλλο σωματίδιο), τότε το ηλεκτρόνιο του μπορεί να μεταπηδήσει σε άλλη επιτρεπόμενη τροχιά υψηλότερης ενέργειας (διέγερση).
Η ενέργεια που απαιτείται για τη διέγερση του ατόμου ονομάζεται ενέργεια διέγερσης.
Η διεγερμένη κατάσταση διαρκεί ελάχιστα δισεκατομυριοστά του δευτερολέπτου και στην συνέχεια το ηλεκτρόνιο επανέρχεται στην θεμελιώδη κατάσταση (αποδιέγερση) είτε απευθείας, με ένα άλμα είτε με περισσότερα από ένα διαδοχικά άλματα.
Κάθε μετάπτωση του ηλεκτρονίου συνοδεύεται από την εκπομπή ενός φωτονίου η ενέργεια του οποίου ισούται με την διαφορά της ενέργειας των δύο διαδοχικών ενεργειακών σταθμών στις οποίες βρέθηκε το ηλεκτρόνιο.
Η συχνότητα του φωτονίου που εκπέμπεται μπορεί να βρεθεί από την χρήση του τύπου Εφωτ=hν => Εφωτ= [Εηλεκτονίου τελική - Ε ηλεκτρονίου αρχική] = hν => ν=Εφωτ/h
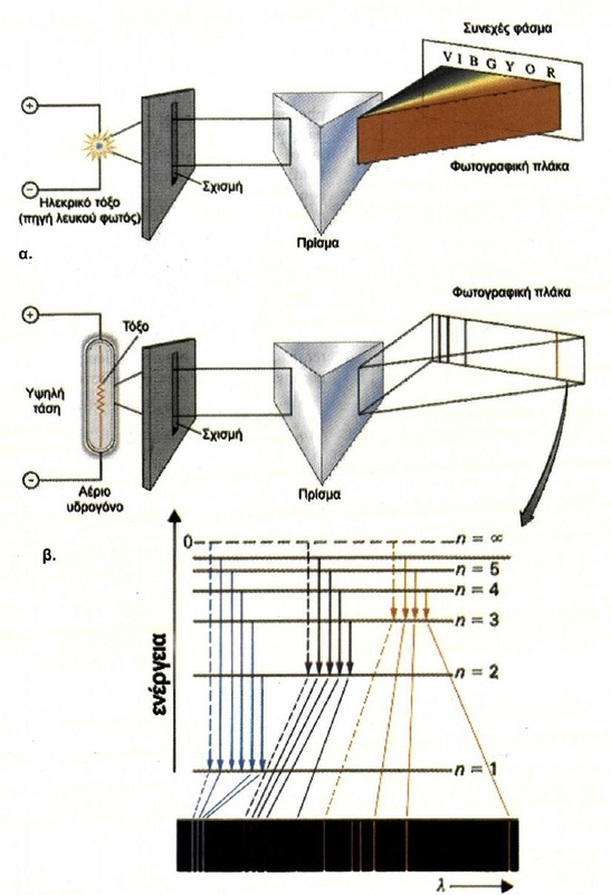
Φάσμα εκπομπής ονομάζουμε το φάσμα ακτινοβολίας που εκπέμπει μια φωτεινή πηγή.
Τα φάσματα εκπομπής είναι είτε γραμμικά είτε συνεχή
Συνεχές φάσμα: περιέχει όλα τα μήκη κύματος του ορατού φωτός π.χ ανάλυση λευκού φωτός πάνω σε πρίσμα και αποτύπωση τους σε φωτογραφική πλάκα
Γραμμικό φάσμα: περιέχει ορισμένα μήκη κύματος
Άρα γίνεται κατανοητό ότι από την διέγερση και αποδιέγερση του ατόμου του ηλεκτρονίου θα υπάρχουν φωτόνια που εκπέμπονται με συγκεκριμένα μήκη κύματος και άρα το φάσμα εκπομπής του θα είναι γραμμικό.
Ανοίξτε μαζί με την προσομοίωση και το παρακάτω φύλλο εργασίας και απαντήστε στις ερωτήσεις.
Ε1=-2,18 10-18 j (ελάχιστη ενέργεια)
Διεγερμένη κατάσταση ενός ατόμου ονομάζεται η κατάσταση η οποία έχει υψηλότερη ενέργεια από την θεμελιώδη. στο άτομο του υδρογόνου διεγερμένες καταστάσεις είναι όλες οι ενεργειακές στάθμες που έχουν n>1 δηλαδή Ε2, Ε3 κ.ο.κ (στιβάδες L, M, N ..)
H ενέργεια του ηλεκτρονίου σε μια διεγερμένη κατάσταση μπορεί να εκφραστεί σε συνάρτηση με την ενέργεια του ηλεκτρονίου στη θεμελιώδη κατάσταση Ε1.
Ισχύει Εn= - 2,18 10-18 /n2 όπου n = 2,3,4...
Aν το άτομο του υδρογόνου που βρίσκεται στη θεμελιώδη κατάσταση (n=1) απορροφήσει ενέργεια (για παράδειγμα με απορρόφηση ακτινοβολίας ή με κρούση με άλλο σωματίδιο), τότε το ηλεκτρόνιο του μπορεί να μεταπηδήσει σε άλλη επιτρεπόμενη τροχιά υψηλότερης ενέργειας (διέγερση).
Η ενέργεια που απαιτείται για τη διέγερση του ατόμου ονομάζεται ενέργεια διέγερσης.
Η διεγερμένη κατάσταση διαρκεί ελάχιστα δισεκατομυριοστά του δευτερολέπτου και στην συνέχεια το ηλεκτρόνιο επανέρχεται στην θεμελιώδη κατάσταση (αποδιέγερση) είτε απευθείας, με ένα άλμα είτε με περισσότερα από ένα διαδοχικά άλματα.
Κάθε μετάπτωση του ηλεκτρονίου συνοδεύεται από την εκπομπή ενός φωτονίου η ενέργεια του οποίου ισούται με την διαφορά της ενέργειας των δύο διαδοχικών ενεργειακών σταθμών στις οποίες βρέθηκε το ηλεκτρόνιο.
Η συχνότητα του φωτονίου που εκπέμπεται μπορεί να βρεθεί από την χρήση του τύπου Εφωτ=hν => Εφωτ= [Εηλεκτονίου τελική - Ε ηλεκτρονίου αρχική] = hν => ν=Εφωτ/h
Φάσμα εκπομπής ονομάζουμε το φάσμα ακτινοβολίας που εκπέμπει μια φωτεινή πηγή.
Τα φάσματα εκπομπής είναι είτε γραμμικά είτε συνεχή
Συνεχές φάσμα: περιέχει όλα τα μήκη κύματος του ορατού φωτός π.χ ανάλυση λευκού φωτός πάνω σε πρίσμα και αποτύπωση τους σε φωτογραφική πλάκα
Γραμμικό φάσμα: περιέχει ορισμένα μήκη κύματος
Άρα γίνεται κατανοητό ότι από την διέγερση και αποδιέγερση του ατόμου του ηλεκτρονίου θα υπάρχουν φωτόνια που εκπέμπονται με συγκεκριμένα μήκη κύματος και άρα το φάσμα εκπομπής του θα είναι γραμμικό.
Ανοίξτε μαζί με την προσομοίωση και το παρακάτω φύλλο εργασίας και απαντήστε στις ερωτήσεις.
| bohr_model__.docx | |
| File Size: | 52 kb |
| File Type: | docx |
Για την καλύτερη κατανόηση της ατομικής θεωρίας του Μπορ,επιλέξτε τις παρακάτω προβολές κινουμένων σχεδίων. Πατήστε τον σύνδεσμο ΙΙ ακολουθήστε τον μέχρι εκεί που λέει multi electron atoms, για μια επισκόπηση του κεφαλαίου στην αγγλική γλώσσα με την βοήθεια animation.
Για να πειραματιστείτε και να γνωρίσετε καλύτερα την θεωρία του Bohr πατήστε τον σύνδεσμο ΙΙΙ και ανοίξτε ταυτόχρονα το παρακάτω φύλλο εργασίας
Για να πειραματιστείτε και να γνωρίσετε καλύτερα την θεωρία του Bohr πατήστε τον σύνδεσμο ΙΙΙ και ανοίξτε ταυτόχρονα το παρακάτω φύλλο εργασίας
| bohr_mcgraw.docx | |
| File Size: | 17 kb |
| File Type: | docx |
Για να ολοκληρώσετ μια ιστορική επισκόπηση της θεωρίας για την δομή του ατόμου, πατήστε στον σύνδεσμο και στην σελίδα που εμφανίζεται πατήστε στα δεξιά σας εκεί που λέει χρησιμοποιώ την επιλογή προεπισκόπηση. Όταν ολοκληρώσετε την περιηγησή σας από την ενότητα επιστήμονες και από την ενότητα σημαντικούς ιστορικούς σταθμούς της θεωρίας για την δομή του ατόμου, απαντήστε το αντίστοιχο κουίζ
Ανοίξτε το παρακάτω αρχείο το οποίο περιέχει ερωτήσεις επανάληψεις
| bohr.docx | |
| File Size: | 220 kb |
| File Type: | docx |
Μπορείτε να κάνετε επανάληψη σε ότι έχετε αναγνώσει ως τώρα με την βοήθεια της παρακάτω προβολής.
